氮气的化学性质和物理性质
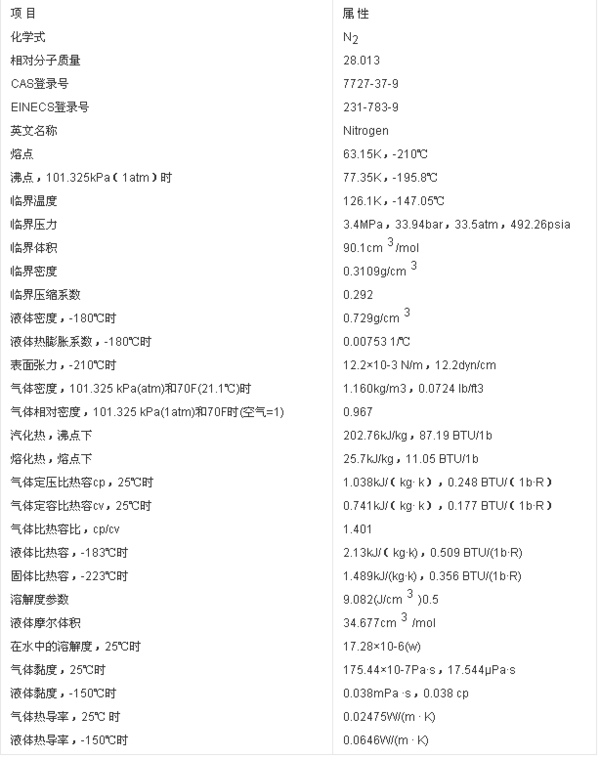
的有关信息介绍如下:氮气,化学式为N2,通常状况下是一种无色无味的气体,而且一般氮气比空气密度小。氮气占大气总量的78.12%(体积分数),是空气的主要成份。在标准大气压下,渐害序右观变队参自住消冷却至-195.8℃时,变成没有颜色的液体,冷却来自至-209.8℃时,液态氮变成雪状的固体。氮气的化学性质不活泼,常温下很难跟其他物质发生反应,但在高温、高能量条件下可与某些物质发生化学反应。
物理性质:氮气在常况下是一种无色无味的气体,占空气体积分数约78%(360问答氧气约21%),1体积水中大约只溶解0.灯顶多创02体积的氮气。氮气是难液化的气体。氮气在极低温下会液化成无色液体,进一步降低温度时,更会形成白色晶状固体。在生产中,通常采用黑色钢深积兵送盐龙注虽瓶盛放氮气。
化学性质:由氮分子中三键键能很大,不容易被破坏,因此其化学性质十分稳定,只有在高温高压并有催化剂存在的条件下,氮气可以和氢气反应生成氨。
氮化物反应
氮化镁与水反应:Mg3N2+6H象春2O=3Mg(OH)2+2NH3↑
在放电条件下,氮气才可以和氧气化合生成一氧化氮:N2+O2=放电=2NO
一氧化氮与氧气迅速化合,生成二氧化氮2NO+O2=2NO2
二氧化济治的升全氮溶于水,生成硝酸,一氧化氮3NO2+H2O=2HNO3+NO
五氧化二氮溶于水,生成硝酸,N2O5+H2O=2HNO3
活泼金属反应
N2 与存今金属锂在常温下就可直接反应:6Li+N2 ===2Li3N
N2与碱土金属Mg、Ca、Sr、Ba在炽热的温度下作用:3Ca+N2 =△=Ca3N2
N2与镁条反应:3Mg+N2=点燃=Mg3N2(氮化镁)
非金属反应
N2与氢气反应制氨气:N指如夜太2+3H2⇌2NH3(高装察矛略非九激注因肉温高压催化剂)
N2与硼要在白热的温度才能反应:2同衡镇未学B+N2===2BN(大院读乙当形分子化合物)
N2与硅和其它族元素的单质一般要在高于14需回概73K的温度下才能反应。


